¿Qué son los cambios de estado progresivos? ¿Cúales son?

En física se denomina cambio de estado a la evolución de la materia entre varios estados de agregación sin que varíe su composición.Los tres estados de agregación más comunes en la Tierra son el líquido, sólido y gaseoso.
Por las condiciones existentes en la superficie terrestre, sólo determinadas sustancias pueden encontrarse en los tres estados de agregación, como por ejemplo el agua. La mayoría de las sustancias se presentan en un estado concreto, así los metales suelen estar en estado sólido, el oxígeno en estado gaseoso… En este tema vamos a ver los principales cambios de estado progresivos de la materia y cómo se producen.
Cambios de estado
Se denomina cambio de estado a la modificación en el estado de agregación de la materia sin variar sus propiedades. Son por tanto evoluciones de la materia entre varios estados de agregación, sin que ocurra un cambio en su composición. Es importante tener en cuenta que en las transformaciones en la fase de las sustancias, estas no se sufren cambios químicos ni se transforman en otras, sólo cambia su estado físico. Trataremos los cambios de estado entre los tres estados clásicos: sólido, líquido y gas. En la siguiente imagen se muestran los diferentes cambios de estado de la materia:
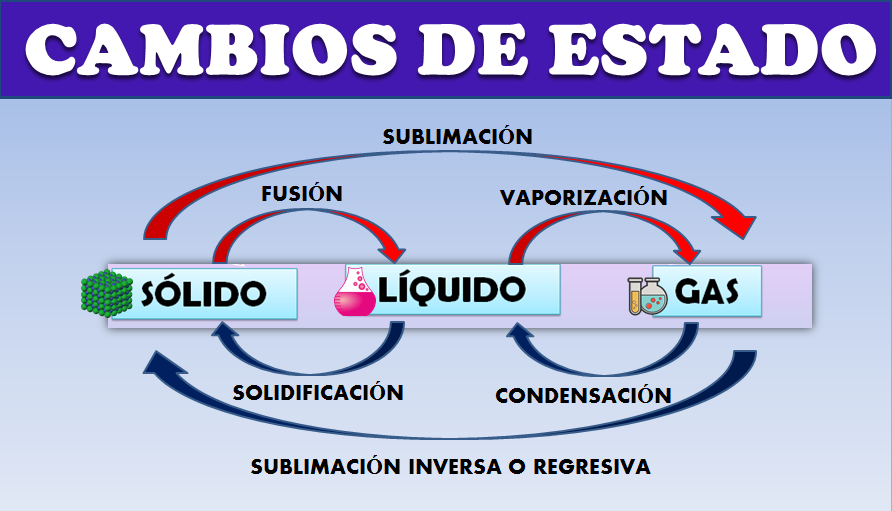
Si en un vaso colocamos un hielo y calentamos, la temperatura aumenta progresivamente y llegaremos a un punto en el que la temperatura permanece constante e invariable y justo en ese momento el hielo empieza a fundirse, en ese momento se está produciendo el cambio de estado de sólido a líquido.
Los cambios de estado se producen al modificar la temperatura (aumentando o disminuyendo) y/o la presión. Según la teoría cinético-molecular al aumentar la temperatura de una sustancia aumenta la energía cinética de sus partículas, por lo que adquieren mayor movilidad y se vencen las fuerzas de cohesión:
-En los sólidos la vibración ocurre con violencia y origina una ruptura de la estructura.
-En los líquidos el aumento de temperatura ocasiona una mayor velocidad de las particular permitiendo que puedan escapar al aire.
Mientras se produce el cambio de estado la temperatura se mantiene constante, ya que en los cambios que requieren aumento de temperatura, la energía se emplea en la ruptura de enlaces y en los cambios que necesitan un enfriamiento, éste produce una reorganización de las partículas.
Video explicativo de los cambios de estado de la materia
A continuación puedes ver un video con los cambios de estado de la materia.
Tipos de cambio de estado
Hay dos tipos fundamentales de cambios de estado
–Cambios de estado progresivos: fusión, vaporización y sublimación progresiva.
–Cambios de estado regresivos: condensación, solidificación y sublimación inversa.
Cambios de estado progresivos
Los cambios de estado progresivos se producen cuando las sustancias absorben calor, por lo que es necesario un aporte de energía para que se produzcan:
-El cambio de sólido a líquido que se denomina fusión
-El paso de líquido a gas llamado vaporización
– El paso de sólido a vapor sin pasar por el líquido que recibe el nombre de sublimación progresiva.
Explicamos todos estos cambios de estado progresivos a continuación
Fusión
La fusión es el paso de materia sólida a materia líquida al aumentar la temperatura de un sólido hasta su punto de fusión. Se trata de un proceso endotérmico (absorbe energía) que necesita un aporte de calor. Ejemplo: derretir mantequilla, fundir chocolate, derretir helados…
Cuando calentamos un sólido, en este proceso de calentamiento, llega un momento en que la temperatura deja de elevarse y permanece constante, esa es la temperatura de fusión, que es la temperatura a la que se produce el cambio de estado.

Vaporización
La vaporización es un proceso físico en el que se produce el paso de líquido a gas. Se trata de un proceso endotérmico (absorbe energía) que necesita un aporte de calor. Ejemplo: paso de agua líquida al estado de vapor…
La vaporización es un fenómeno que puede ocurrir de dos formas:
- Ebullición: el proceso de ebullición consiste en el paso de la fase líquida a la fase gaseosa aportando calor. Cuando calentamos un líquido , en este proceso de calentamiento, llega un momento en que la temperatura deja de elevarse y permanece constante, esa es la temperatura de ebullición,
- Evaporación: es el paso de líquido a gas y ocurre cuando un líquido se evapora de manera natural sin necesidad de aportar calor o cambiar sus condiciones

Sublimación
La sublimación es el paso del estado de sólido a gaseoso sin pasar por el estado líquido. Este proceso ocurre cuando las moléculas que componen el sólido adquieren la energía suficiente para vencer las fuerzas de atracción que las mantienen unidas entre ellas y logran escapar al estado gaseoso.
La palabra sublimación procede de la palabra sublimatio, que se traduce como “elevación”, del verbo latino sublimare “enaltercer o elevar”.
Ejemplo de sublimación es el hielo seco . A temperatura ambiente, el hielo elaborado con dióxido de carbono, comprimido y congelado recupera su forma gaseosa original. En el planeta Marte se encuentra en estado natural y sublima cuando la superficie le llega la luz solar durante la primavera.

